近期較為大眾所知悉的藥物莫過於苯二氮平類藥物(benzodiazepines)與巴比妥類藥物(barbiturates),由於兩者皆具有抗焦慮、鎮靜、及安眠的效果,因此很容易被濫用,尤其是前者。
苯二氮平類藥物為目前臨床上常見的鎮靜安眠類藥物之一,在使用上尤須注意其所使用的劑量,使用劑量不足而未能達到治療效果,或使用劑量過高而帶來嚴重的副作用,都不是治療上樂見的結果。特定的苯二氮平類藥物使用劑量無論在臨床上或是專利權的保護中皆格外重要,亦是專利侵權訴訟中熱門爭點之一。因此,本文藉由Tyco Healthcare Group LP v. Mutual Pharmaceutical Co., Inc.(Fed. Cir. 2011)案件[1]來探討苯二氮平類藥物使用劑量的顯而易見性。

案件背景
本案被告Mutual學名藥廠因為向食品藥物管理局 (FDA) 提出了Restoril® 7.5毫克 (成分為替馬西泮temazepam,使用劑量為7.5毫克,是一種苯二氮平類藥物) 的學名藥許可之簡易新藥上市程序(ANDA),原告美商泰可醫療保健集團公司 (Tyco Healthcare Group LP) 於是向美國紐澤西州 (the District of New Jersey) 的地方法院提出專利侵權訴訟,主張被告Mutual學名藥廠侵害了系爭專利的申請專利範圍第1項及第2項,Mutual學名藥廠則主張原告美商泰可醫療保健集團公司的專利顯而易見,地方法院經過判決後認定被告Mutual學名藥廠無文義侵權,且系爭專利因為顯而易見而無效。原告美商泰可醫療保健集團公司不服地方法院的判決,所以提出上訴。
A型γ-胺基丁酸受體與苯二氮平類藥物
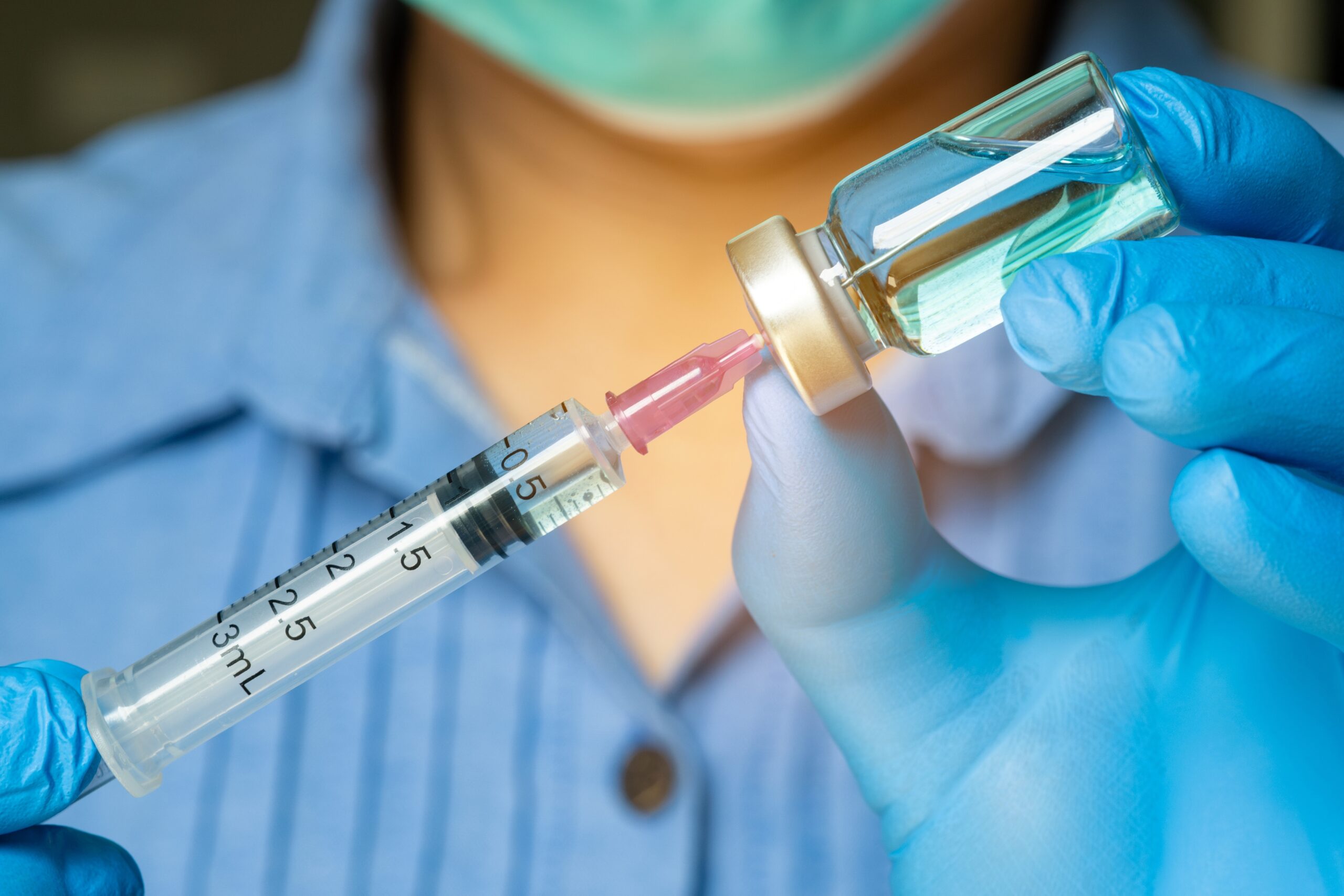
A型γ-胺基丁酸受體 (gamma aminobutyric acid A receptor,GABAA receptor,圖1) 為一種氯離子(chloride ion) 通道型的受體,其由五部分所組成,分別為兩個α1、兩個β2及一個γ2。於A型γ-胺基丁酸受體上有γ-胺基丁酸受體的結合位置 (GABA site),以及苯二氮平類藥物的結合位置 (BZD site)。
苯二氮平類藥物可藉由結合A型γ-胺基丁酸受體,使氯離子通道開啟,氯離子的流動得以增加,造成中樞系統的過極化,產生中樞系統的抑制作用,藉此達到臨床上肌肉鬆弛、抗焦慮、鎮靜、安眠、及抗癲癇等治療效果[2]。臨床上,較常見的苯二氮平類藥物有阿普唑侖 (alprazolam) 、二氮平 (diazepam) 、替馬西泮等。
由於苯二氮平類藥物在臨床上須特別注意使用劑量,因此,市面上會有許多不同劑量的商品,例如替馬西泮的商品就有7.5毫克、15毫克、22.5毫克、及30毫克等不同劑量。
本案系爭專利
本案系爭專利為美國專利第5,211,954號(’954專利)[3]。系爭專利之申請專利範圍總共有2項,2項皆為獨立項,列出如下:
- A hard gelatin capsule containing a temazepam formulation consisting essentially of 6 to 8 milligrams of crystalline temazepam having a surface area of from 0.65 to 1.1 m 2 /g and 95 % of the temazepam having a particle size of less than 65 microns in admixture with a pharmaceutically acceptable carrier therefor.
- A hard gelatin capsule containing a temazepam formulation consisting essentially of 7.5 milligrams of crystalline temazepam having a surface area of from 0.65 to 1.1 m 2 /g and 95 % of the temazepam having a particle size of less than 65 microns in admixture with a pharmaceutically acceptable carrier therefor.
系爭專利申請專利範圍第1項及第2項皆是以替馬西泮為治療藥物,但兩者的使用劑量不同,前者為6至8毫克,後者為7.5毫克,後者即為本案之Restoril® 7.5毫克,於1991年於美國核准上市。另外,第1項及第2項皆主張有結晶型 (crystalline) 之替馬西泮特定的表面積 (surface area) 為0.65至1.1 m 2 /g。
本案相關先前技術
為了挑戰系爭專利申請專利範圍的顯而易見性,使系爭專利申請專利範圍無效,本案的被告Mutual學名藥廠提出了一些先前技術,其中,具有代表性的先前技術列出於下:
- Restoril® 15 毫克與Restoril® 30 毫克:該兩藥物為早於本案Restoril® 7.5 毫克專利優先日前已存在之不同使用劑量的Restoril。
- 1983年的英國國家處方集 (British National Formulary):1983年的英國國家處方集中列出了替馬西泮的適應症 (indications)、相關注意事項及副作用、與使用劑量。替馬西泮可以用於治療失眠症 (insomnia),其相關使用劑量為10至30 毫克 (老年患者使用劑量為5至15毫克) 嚴重失眠症時可增加到60毫克,服用藥物的時間為睡前30分鐘。
原告美商泰可醫療保健集團公司亦提出了一項先前技術反駁被告Mutual學名藥廠如下:
- 1976年的Nicholson論文發表:該論文發表中揭露給予試驗者替馬西泮的使用劑量為10毫克與20毫克,10毫克的替馬西泮顯著地減少了試驗者入睡所需的時間,但微小地,或沒有增加試驗者的睡眠總時間。
- 1979年的Nicholson論文發表:該論文發表中揭露給予試驗者替馬西泮的使用劑量為20毫克。20毫克的替馬西泮有效地改善了失眠症,其顯著地減少了試驗者入睡所需的時間及增加了試驗者的睡眠總時間。
文義侵權部分
地方法院認為由於被告Mutual學名藥廠的Restoril® 7.5 毫克學名藥中,結晶型之替馬西泮特定的表面積為2.2 m 2 /g,與系爭專利所主張的0.65 至 1.1 m 2 /g不同,故被告Mutual學名藥廠並無文義侵權。此部分並無進一步爭議。
系爭專利Restoril® 7.5 毫克的使用劑量是否顯而易見
地方法院認為被告Mutual學名藥廠已提出有力的兩先前技術,Restoril® 15 毫克與1983年的英國國家處方集中所揭露之老年患者使用劑量為5至15毫克的部分,藉由該兩先前技術之組合可使該發明所屬領域中具通常技術之人將替馬西泮的使用劑量降低,因此,Restoril® 7.5 毫克的使用劑量顯而易見。
上訴人美商泰可醫療保健集團公司抗辯地方法院的認定有誤,其主張1983年的英國國家處方集中之揭露非直接指引該發明所屬領域中具通常技術之人使用5至15毫克的劑量、先前技術Nicholson的兩論文發表對於使用較低劑量具反向教示、及系爭專利存有輔助性判斷因素 (secondary consideration) ,因此,系爭專利Restoril® 7.5 毫克非顯而易見。
上訴法院認為1983年的英國國家處方集中之老年患者使用劑量5至15毫克的揭露已足以指引該發明所屬領域中具通常技術之人朝向較低的替馬西泮使用劑量。且上訴人美商泰可醫療保健集團公司對於Nicholson的兩論文發表認定有誤,1976年的Nicholson論文發表未反對使用較低的劑量 (即替馬西泮10毫克),1979年的Nicholson論文發表更僅討論了替馬西泮20毫克,該兩論文發表並未對於Restoril® 7.5 毫克的使用劑量有反向教示。系爭專利具有輔助性判斷因素中的無法預期之結果 (unexpected results) 與商業上的成功 (commercial success) 部分無法克服系爭專利之顯而易見。故最終,上訴法院仍維持了地方法院對於系爭專利Restoril® 7.5 毫克的使用劑量顯而易見的認定。
小結
苯二氮平類藥物在臨床使用劑量上須特別注意,因此會有許多不同的劑量產品,本案為Restoril® 7.5毫克的使用劑量。在本案判決中,我們可以知悉由於Restoril® 7.5毫克上市前已有Restoril® 15毫克與Restoril® 30毫克,以及1983年的英國國家處方集已揭露老年患者使用劑量為5至15毫克,該些先前技術已足以明確地指引該發明所屬領域中具通常技術之人朝向降低替馬西泮的使用劑量,因此,上訴法院與地方法院一致認為系爭專利Restoril® 7.5毫克的使用劑量顯而易見。
另外,本案上訴人美商泰可醫療保健集團公司有主張輔助性判斷因素中的無法預期之結果及商業上的成功,關於較詳細的輔助性判斷因素相關議題可參考第328期《淺述藥物專利顯而易見性之輔助性判斷因素》。
【本文僅反映專家作者意見,不代表本報立場。】
|